在所有的电池负极材料中金属锂具有最低的密度,最高的理论电压,最好的电子电导,同时其电化学容量达3860 mAh/g,所以近十几年来以金属锂为基础的电池主导了高性能电池的发展。水系电解质锂 空气电池很早就有人研究,电池放电反应方程为:4Li + O2 + 2H2O → 4LiOH(E? =3.35V),放电过程中,金属锂、水和氧气被消耗产生LiOH,由于金属表面生成了一层保护膜而阻碍了腐蚀反应的快速发生。但是在开路状态下和低功率 状态下,金属锂的自放电率相当高,伴随着锂的腐蚀反应: Li + H2O → LiOH + 1/2H2,该反应的发生降低了电池负极的库仑效率,同时也带来了安全上的问题。综合考虑到实用性、成本和安全性,水系锂空气电池非金属空气电池的首选。
有机系锂/空气电池在当前诸多的电池体系中具有最高的能量密度,排除氧气后的能量密度达到惊人的11140 Wh/kg,高出现有电池体系1-2个数量级。本文综述了新型有机系锂空气(氧气)电池的研究进展,并对发展趋势和存在的关键进行了分析和展望。
1 锂空气电池的反应机理
我们现在说的锂/空气电池通常是指有机系电解液锂空气电池(下面我们提到的锂空气电池都是这种有机系列的),这是近几年刚刚发展起来的新型电源体系,目前在国内外从事锂/空气电池研究的很少。1996年,K. M. Abraham等人在 J. Electrochem. Soc.上首次报道了有机系列电解液锂/空气电池[1]。有别于常规的铝/空气电池和锌/空气电池的水系电解液电池体系,锂/空气电池是一种全新的金属/空气电池。相对于使用水系和类水系电解液的传统空气电池而言,使用有机系列电解液或全固态电解质可以获得更高的额定电压(理论值是2.9-3.1 V),同时锂/空气电池的能量密度也远高于其他金属/空气电池,它的工作原理是基于以下两个反应:
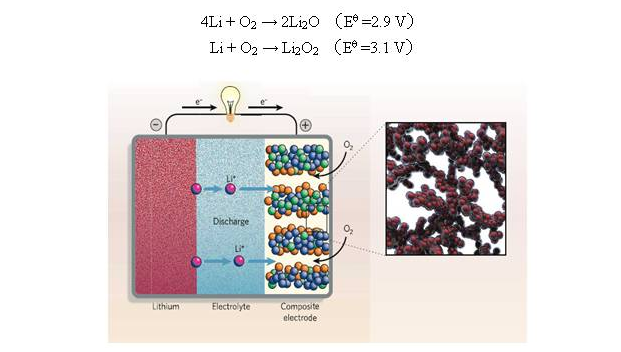
图1 锂空气电池工作原理示意图
如图1所示,首先,氧气在多孔空气电极表面还原成O2-或O22-,接着与电解液中的Li+结合生产产物Li2O2或Li2O。由于过氧化锂和氧化锂均不溶解在有机电解液中,因此放电产物只能在有氧负离子或过氧负离子的空气电极上沉积,在阳极过量的情况下,放电的终止是由于放电产物堵塞空气电极孔道所致。
按第一个反应计算,电池开路电压为2.91 V,理论能量密度为5200 Wh/kg,而在实际应用中,氧气由外界环境提供,因此排除氧气后的能量密度达到惊人的11140 Wh/kg,高出现有电池体系1-2个数量级,在军用和民用的高能量密度领域中具有重要的应用前景。
2 研究面临的主要困难
目前制约其发展和应用的主要有以下几个方面:
(1)由于锂空气电池是在敞开环境中工作,通常的有机液体电解质存在容易挥发的问题,从而影响了电池的放电容量、使用寿命及电池的安全性。
(2)在空气中使用时,锂空气电池需要解决如何防止气体进入电池的问题。有机液体电解质体系容易吸收水分而导致锂负极在空气中腐蚀的问题;另外,H2O和CO2的存在会使产物锂的氧化物减少,而反应生成的Li2CO3不具有电化学可逆性,从而导致锂空气电池的循环性能下降。
(3)在没有催化剂存在时,氧气在阴极的还原非常缓慢,为降低正极反应过程的电化学极化,必须加入高效的氧还原催化剂,而经典的氧还原催化剂 钛氰钴、铂及其合金价格昂贵,不利于工业化生产。另外,由于锂空气电池的充电电压很高,一般都在4.5 V左右或者更高,使用合适的催化剂也有利于减小充电电压。因此寻找廉价高效的氧还原催化剂迫在眉睫。
如何解决上述问题,成为了锂空气电池能否得到成功应用的关键,而目前锂空气的相关研究也主要针对以上几个方面进行。
3 锂空气电池的相关研究
锂/空气(氧气)电池的研究刚刚起步,有关报道很少。该项目的研究得到了美国航天局和美国军事实验室的大力支持。全球研究锂/空气电池的小组 主要有:锂/空气电池的创始人K. M. Abraham,美国军事实验室的J. Read,英国的P. G. Bruce,日本的Kuboki,美国的S. S. Sandhu,Hui Ye等。他们的研究主要集中在电池的工作机理和电解液对电池性能的影响等方面。超高的能量密度及广阔的应用前景,吸引了越来越多的人投身到该领域的研究之中,近期更有愈演愈烈之势。
K. M. Abraham在首次报导锂/空气电池的文章中介绍了以凝胶聚合物(PAN – PVDF)加有机溶剂和锂盐作为电解质的锂/空气电池[1],该电池开路电压接近3 V,工作电压在2.0 – 2.8 V之间。无催化剂时,电池电压平台为2.4-2.5 V左右,容量达1400 mAh/g,远高于常规的锂离子电池体系。以酞菁钴作为空气电极的催化剂,具有良好的库仑效率并能循环三圈。作者认为放电机理是锂离子和氧气在碳基空气电极上生成过氧化锂,而空气电极中的气孔被反应产物Li2O2沉积阻塞而最终导致放电结束。
J.Read在锂/空气电池放电机理、电极材料以及电解液组成方面做了大量工作[3-5]。锂/空气电池与水系金属/空气电池的最大区别在于其放电产物是沉积在阴极而不是阳极。由于过氧化锂和氧化锂均不溶解在有机电解液中,因此放电产物只能在有氧负离子或过氧负离子的空气电极上沉积。在阳极过量的情况下,放电的终止是由于放电产物堵塞空气电极孔道所致。J. Read详细地研究了空气电极材料、电解液组成、氧分压和氧溶解能力对放电容量、倍率性能以及循环性的影响,认为电解液组成对电池性能以及放电产物沉积行为有极大影响,并提出以醚类溶剂作为锂/空气电池的电解液,所得容量达2800 mAh/g。
P. G. Bruce在锂/空气电池充电机理研究上做出重大贡献,并验证了反应具有可逆性。研究结果认为反应2Li+ +2e- + O2→ Li2O2为可逆反应,当放电产物为过氧化锂时,电池具有可充放性,实现了50次循环,容量为600 mAh/g [6]。同时,作者研究了不同的经典氧还原催化剂对容量以及对电池循环性能的影响,结果表明Fe2O3作为催化剂时拥有最高的首次充放电容 量,Fe3O4、CuO、CuFe2O4作为催化剂时具有最好的容量保持率,而使用Co3O4作为催化剂时兼有良好的放电容量和循环性能,并且具有最低的 充电电压4 V [7]。另外,作者比较了一系列经典锰的氧化物催化剂对电池充放电的影响,结果表明α-MnO2 纳米线催化的锂空气电池拥有最高容量为3000 mAh/g,循环8圈后容量仍保持在2000 mAh/g,这也是目前得到的最佳二次锂空气电池[8](见图2)。
Vincent Mark B等人[9] 采用一种新的方法合成了MnOOH化合物,并将其作为锂/空气电池的氧还原催化剂用在Yardney锂空气电池中进行测试,较之未加催化剂的电池比容量提高了38%,达2200 mAh/g,取得了较好的催化效果。

图2 典型的锂空气电池充放电曲线
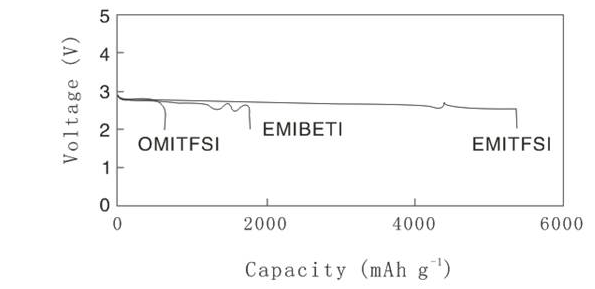
图3 空气气氛下离子液体作为锂空气电池电解液时充放电曲线
在空气气氛下工作时,电解液的挥发和吸水成为亟待解决的问题。东芝公司的Kuboki等人首次报告了用疏水的锂离子液体来防止金属锂与水汽接触时发生水解,这样可以延长锂/空气电池的寿命[10]。另外,与通常的有机液体锂电解质不同,离子液体电解质的蒸汽压可以忽略不计,所以可以在温和的敞开环境中使用。Kuboki等人研究了湿度、温度对电池放电过程的影响,作者认为长时间的放电没有对放电行为造成明显的影响,组装的电池在空气中工作了56天。作者同时对比了使用有机电解质时的电化学性能,与其他电解质相比,离子液体表现出最好的性能,如图3所示,其放电容量高达5360 mAh/g。
Hui Ye等人研究了多种离子液体的电化学性能,同时筛选出电化学性能最佳的吡咯型离子液体,并将这种离子液体制备成胶态聚合物电解质,该电解质应用在锂/空气电池上首次充放电容量为900 mAh/g,工作电压为2.5 V。放电过程中,Li和电解质界面的阻抗随着放电的进行变得很大,这可能是由于O2穿过了电解质液面和Li片发生反应,在Li片表面上生成了Li2O,这也可能是放电终止的另外的一个重要原因[11]。
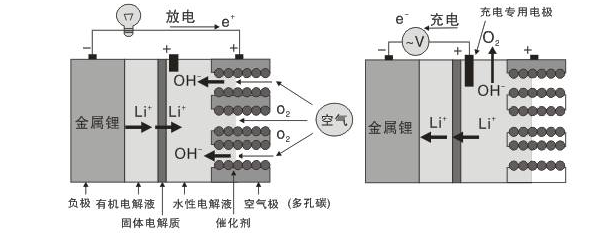
图4 新结构“锂空气电池”的构成。左侧为放电,右测为充电
最近日本产业技术综合研究所发布相关的锂空气电池的设计。如图4所示,只在金属锂的负极使用有机电解液,正极的空气电极使用水性电解液,之间用只能通过锂离子的固体电解质隔开以防止两电解液发生混合,而且能促进电池发生反应。这样,结合有机系和水系锂空气电池的优点,该电池通过放电反应生成的不是固体氧化锂(Li2O),而是易溶于水性电解液的氢氧化锂,这样就不会引起空气极的碳孔堵塞。另外,由于水和氮等无法通过固体电解质隔膜,因此不存在和负极的锂金属发生反应的危险。使用了此次新开发的碱性水性电解质凝 胶的锂空气电池在空气中以0.1 A/g的放电率放电时,放电容量约为9000 mAh/g。另外,充电容量也约达到 9600 mAh/g。与此前报道的原锂空气电池的容量(700~3000 mAh/g)相比,放电容量大幅提高。而使用碱性水溶液代替碱性水溶性凝胶后,在空气中以0.1 A/g的放电率放电时,可连续放电20天,放电容量约为50000 mAh/g(图5)。
新的锂空气电池没电时也无需充电,只需更换正极的水性电解液,通过卡盒等方式更换负极的金属锂就可以连续使用。这是一种新型燃料电池,名为“金属锂燃料电池”。理论上30 kg金属锂释放的能量与40 L汽油释放的能量基本相同。如果从用过的水性电解液中回收空气极生成的氢氧化锂(LiOH),很容易重新生成金属锂,可作为燃料进行再利用。
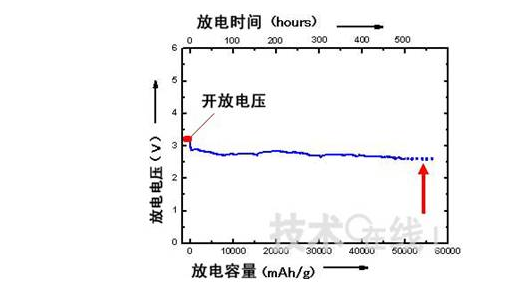
图5 新结构“锂空气电池”的长时间连续放电曲线
对锂空气电池理论方面的研究也有报道。S.S. Sandhu等人通过数学计算构建数学模型等方法研究了锂空气电池的可逆反应电压、热效率、孔隙率和放电容量的关系等,而得到的放电容量和实验值相近 [12,13]。J. P. Zheng等人也在锂/空气电池理论比能量的相关研究中取得了一定进展[14]。
锂空气电池的专利日益增多。K. M. Abraham 曾报道了基于PAN-PVDF体系的锂氧电池体系(专利号:US 5561004),其他的专利则只包括Eltron公司等在离子液体(US 4804448)和正极材料(US 71477967)方面的一些工作,Johnson, Lonnie G. 也报道了锂空气电池制造方法。在最近的报道中,由于锂空气电池巨大能量密度,越来越多的公司企业都投身于锂空气的开发中,相关的专利报道与日俱增。
4 研究展望
面对通常的有机液体电解质体系存在容易挥发和吸收水分而导致锂负极在空气中腐蚀的问题,疏水型离子液体虽然可以在一定程度上减小锂的腐蚀,但即使是疏水的离子液体在空气中使用时也会混进少量的水。与此同时,离子液体不含锂,作为电解质在锂电池中使用时需要加入锂盐,而大部分的锂盐是非常容易吸水的(比如 LiTFSI),所以这也给离子液体的使用带来了新的挑战。在我们最近的研究中,我们使用离子液体-疏水氧化硅复合电解质用于锂空气电池的防水电解质膜能有效的延缓水对锂的腐蚀,在空气中工作放电容量达 4000 mAh/g 以上,但是这不能从根本上防止水的腐蚀,致密的固体电解质有利于锂的保护,防止H2O、CO2、O2到达负极,如果能保证其获得足够的电导率及相关的工艺问题,有望解决作为锂空气电池合适的电解质。
在空气中使用时,锂空气电池需要解决如何防止气体进入电池的问题。CO2的存在会使锂的氧化物减少,反应生成的Li2CO3也不具有电化学可逆性,从而使锂空气电池的循环性能下降。另外,O2透过电解质到达负极,与金属锂反应生成锂的氧化物会覆盖在锂的表面,阻止了放电反应的进一步发生。
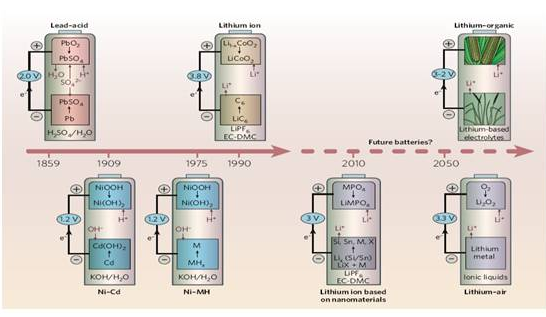
图6 未来清洁电池能源预测
经典的氧还原催化剂钛氰钴、铂及其合金价格昂贵,不利于工业化生产。而MnO2、Co3O4 等廉价的氧还原催化剂有望成为其良好的替代品,通过合成高效的催化剂,有望实现锂空气电池良好的容量保持率。此外,如何通过优化电池结构,获取足够的空隙 率,这些问题的解决也是使锂空气电池能够得到实际应用的关键之一。
锂/空气电池作为一种环境友好的新型电池体系,无疑具有广阔的应用潜力,有望在未来广泛使用(图6)。
5 小结
巨大的能量密度决定了锂/空气电池将会在航空和移动能源领域中有广泛应用,如果能成功解决安全、腐蚀问题及其相关材料设计和制备问题,锂/空气电池将会是能源史上的一次重大革命。



